Vacuna rusa Sputnik V presenta documentación en Cofepris
La documentación es para realizar estudios clínicos y obtener autorización
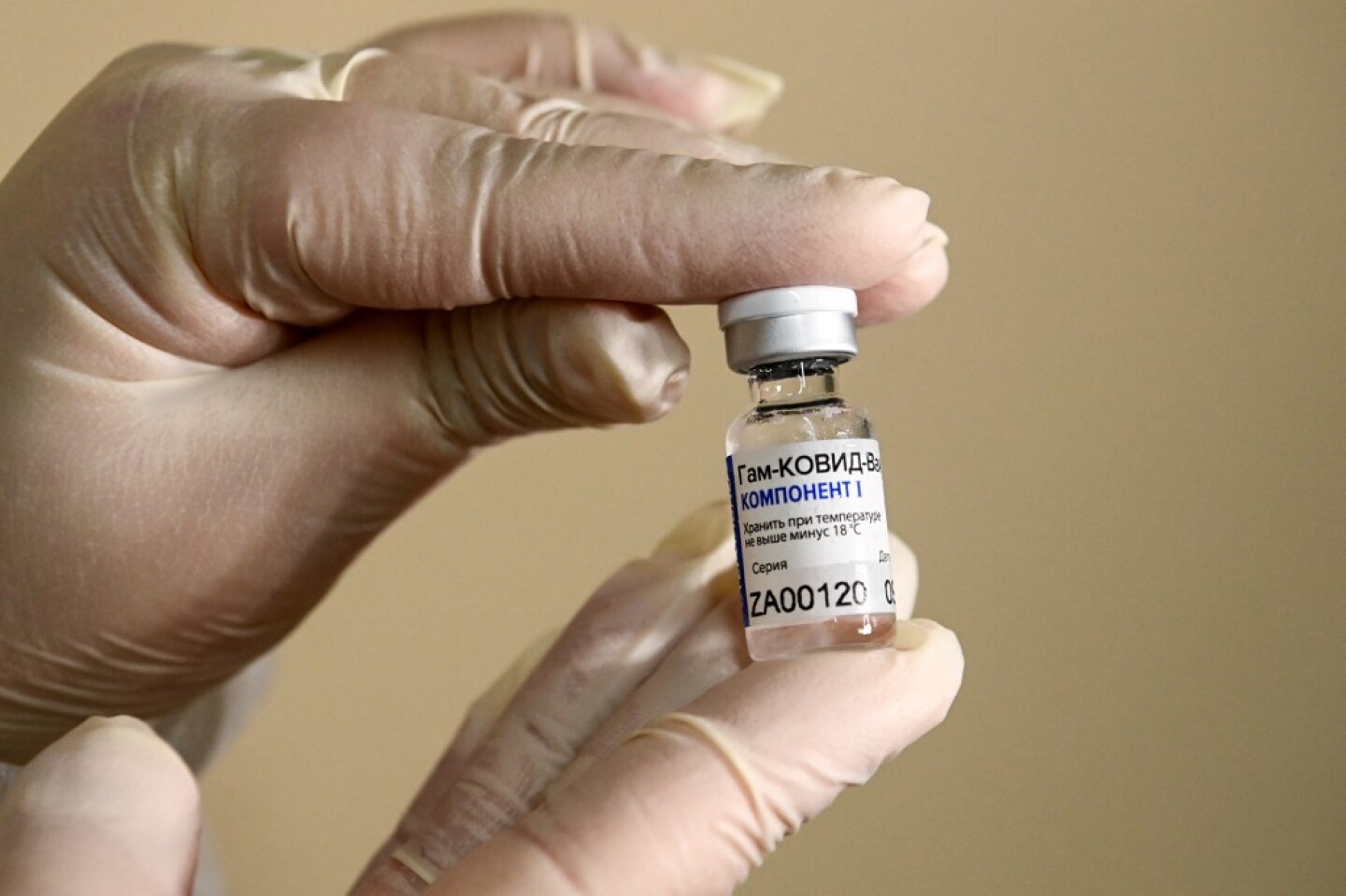
A nurse shows the Sputnik V (Gam-COVID-Vac) vaccine against the coronavirus disease (COVID-19) at a clinic in Moscow on December 5, 2020, amid the ongoing coronavirus disease pandemic. - Russian President has told authorities to begin “large-scale” vaccinations among at-risk populations. The drugs should be made generally available to the Russian public in early 2021. (Photo by Kirill KUDRYAVTSEV / AFP)
/KIRILL KUDRYAVTSEV/AFP
Los fabricantes de la vacuna rusa “Sputnik V” presentaron su documentación en la Comisión Federal para la Protección contra Riesgos Sanitarios (Cofepris) para realizar estudios clínicos y obtener autorización.
“Les comparto que a invitación de México, los fabricantes rusos de la vacuna “Sputnik V” han presentado solicitud y documentación necesaria a la Cofepris para realizar estudios clínicos en nuestro país y obtener la autorización correspondiente. Buena semana”, dijo el canciller Marcelo Ebrard.
En noviembre pasado, Rusia informó que su vacuna “Sputnik V” contra la Covid-19, desarrollada por el centro de investigación Gamaleya de Moscú, tiene una eficacia del 95%.
Se trata de resultados preliminares obtenidos con voluntarios 42 días después de la inyección de la primera dosis. El ministerio ruso de Salud y el Fondo Soberano ruso implicado en el desarrollo de la vacuna.
Además, el pasado 11 de diciembre, el laboratorio británico AstraZeneca y Rusia anunciaron ensayos clínicos conjuntos que combinan sus dos vacunas contra el nuevo coronavirus.
“Anunciamos un programa de ensayos clínicos para evaluar la seguridad y la inmunogenicidad de la combinación de ASD1222, desarrollada por AstraZeneca y la Universidad de Oxford, y Sputnik V, desarrollada por el instituto de investigación Gamaleya”, indicó la antena de AstraZeneca en Rusia. En dicho comunicado se precisaba que los ensayos se realizarán en individuos mayores de 18 años. NR
ES DE INTERÉS
AstraZeneca y Sputnik V van en alianza contra la Covid-19
Afirma Rusia que su vacuna Sputnik V es eficaz en un 95%



